Medicamentele: pro şi contra
December 17th, 2012, Alice-Claudia Gherman 7 comentarii
Tweet
7 comentarii
Tweet
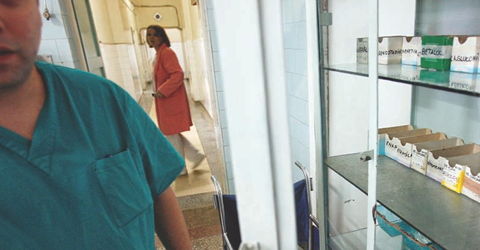
Dacă vesticii au retras unele medicamente din piaţă, când specialiştii lor au constatat că au efecte nocive pentru sănătatea pacientului, de ce nu le-am retras şi noi? Pentru a lămuri lucrurile, ne-am interesat la Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale – ANMDM – de ce şi, mai ales, când se retrage un medicament din piaţă.
De curând, în Franţa a apărut un scandal legat de prezenţa unor numeroase medicamente nocive pe piaţa farmaceutică din Hexagon. În consecinţă, francezii au retras din piaţă o serie de medicamente. Între ele: Actos, un antidiabetic, prezent şi pe piaţa noastră farmaceutică. Specialiştii francezi susţin că antidiabeticul este responsabil de apariţia unor forme de cancer. Această ştire a inflamat imediat presa românească. De ce, la noi, nu a fost retras Actos? Mi-au revenit rapid în minte numeroasele articole ale jurnaliştilor privind efectele nocive şi ale altor medicamente precum Ketotifen, Mabcampath, Methotrexat, Izoniazidă aflate pe lista de medicamente aprobate de ANMDM. Nu mai spun de banalul şi românescul Algocalmin, incriminat şi înfierat de numeroşi ziarişti sau bloggeri, chiar şi după ce a fost trecut pe lista medicamentelor care se dau numai pe bază de reţetă. Aprofundând problema, am descoperit un teren minat cu numeroase păreri pro şi contra. În funcţie de medicament şi de cât de nocive sunt efectele acestuia constatate în unele ţări ale UE. În funcţie de interesul celor care trimit mail-uri de avertizare privind x, y, z medicament în vederea scoaterii lui din piaţă sau a menţinerii acestuia la vânzare. Şi, discutând cu farmacişti, am mai înţeles un lucru: unele medicamente, chiar dacă au efecte adverse, se menţin în piaţă pur şi simplu fiindcă la ora actuală nu există altceva mai eficient pentru tratarea anumitei afecţiuni, iar beneficiile sunt mai importante decât reacţiile adverse. Este cazul Izoniazidei, care tratează, pare-se cu succes, tuberculoza, iar medicamentul se află în farmaciile româneşti în ciuda faptului că, după unii, ar cauza probleme grave ficatului
Dar să revenim. Am întrebat la ANMDM pentru a şti cu exactitate când se scoate un medicament din circuitul farmaceutic. Am aflat, prin vocea dnei farmacist specialist Anca Crupariu, ofiţerul de presă al ANMDM, că există patru cazuri în care un medicament se retrage de pe piaţă: atunci când Comisia Europeană emite o decizie de suspendare temporară sau de retragere definitivă a Autorizaţiei de Punere pe Piaţă (APP) a unui medicament pe întreg teritoriul Uniunii Europene ca urmare a recomandărilor în acest sens formulate de experţii Comitetului pentru Medicamente de Uz Uman (Committee for Medicinal Products for Human Use – CHMP) al Agenţiei Europene a Medicamentului (European Medicines Agency – EMA); în urma unor Alerte Rapide referitoare la calitate şi venite la ANMDM prin Sistemul de Alertă Rapidă – SAR al ţărilor care fac parte din European Economic Area şi alte două organisme de inspecţie farmaceutică; în urma inspecţiilor de supraveghere a calităţii medicamentelor efectuate pe teritoriul României de către inspectorii ANMDM, atunci când se constată neconformităţi faţă de parametrii de calitate cuprinşi în specificaţia medicamentului de uz uman şi, în al patrulea caz, în condiţii de retragere voluntară realizată de către firma deţinătoare de APP, prin autosesizare sau ca urmare a anumitor sesizări din partea pacienţilor. Cu alte cuvinte, dacă un medicament este scos de pe piaţă doar de către una sau două ţări membre ale UE, cum e cazul Actos, retras din Franţa, iar această decizie este una locală şi nu este o decizie emisă de CE la sugestia EMA, atunci România prin ANMDM nu are obligaţia să retragă acel medicament din farmaciile autohtone. Dna farmacist Anca Crupariu ne-a precizat, de asemenea, că: „Orice medicament autorizat de punere pe piaţă poate produce reacţii adverse, fapt cunoscut şi acceptat pe plan internaţional. Apariţia şi manifestarea reacţiilor adverse într-un grad mai mic sau mai mare de gravitate este şi o problemă de reactivitate individuală, ca de altfel şi apariţia altor reacţii adverse decât acelea semnalate în prospect. Reacţiile adverse la medicamente sunt monitorizate şi după autorizarea de punere pe piaţă. În acest context, în prospectul medicamentului se menţionează: Este necesar să informaţi medicul despre orice altă reacţie adversă nemenţionată în acest prospect.” Întrebările care se nasc aici sunt: câţi pacienţi români se mai duc şi spun medicului despre reacţiile adverse? Am cunoscut cazuri de pacienţi care, dacă s-au simţit rău, pur şi simplu nu au mai luat medicamentul şi au schimbat medicul. Câţi dintre medici, preluând informaţiile de la pacient, le transmit mai departe Centrului Naţional de Farmacovigilenţă – cel care colectează datele privind reacţiile adverse şi evaluează din punct de vedere ştiinţific aceste informaţii corelându-le cu consumul de medicamente din teritoriu şi datele privind întrebuinţarea greşită şi abuzul de medicamente la nivel naţional?
Pe site-ul ANMDM există chiar două rubrici unde pot fi trimise sesizări cu privire la reacţiile adverse sau la probleme legate de calitatea medicamentelor, sunt ele suficiente? Greu de răspuns. Cert este că pentru Ketotifen, Mabcampath, Methotrexat, Izoniazidă sau chiar şi Actos nu au existat raportări de reacţii adverse în România care să determine o relaţie clară de cauzalitate între efectul advers şi vreunul dintre medicamentele administrate şi enumerate mai sus care să determine ANMDM să le elimine din lista medicamentelor agreate în piaţa de la noi.
Dacă în cazul medicamentelor sus-menţionate, România nu s-a luat după ceea ce fac alţii – şi poate că este un lucru bun – în ceea ce priveşte analgezicele lucrurile au stat altfel, ne-am aliniat la UE. Este cazul seriei de medicamente a cărei cap de afiş este algocalminul, urmat de quarelin, fabocalm, metamizol solacium, algiotop, algoblock, algozone, alindor, algoremin, metamizol farmacon, novocalmin, sintocalmin şi centralgin. Toate conţin metamizol – algocalminul conţine 500 mg de metamizol per comprimat –, substanţa incriminată în apariţia agranulocitozei – fenomen alergic de tip anafilactic caracterizat prin scăderea numărului celulelor din sânge numite granulocite şi apoi duce la distrugerea măduvei osoase. Riscul apariţiei agranulocitozei a determinat multe state membre UE să restricţioneze utilizarea medicamentelor pe bază de metamizol, iar România a aderat şi ea impunând eliberarea numai pe bază de prescripţie medicală. Imediat, o parte a ziariştilor de la noi au salutat decizia de trecere a algocalminului şi a tuturor comprimatelor pe bază de metamizol de la OTC-uri la medicamente eliberate numai cu reţetă. S-au consumat tone de cerneală şi de spaţiu virtual în care, sprijiniţi de opiniile unor medici, ziarişti sau simpli bloggeri au trecut algocalminul la categoria „otrăvuri”. Toţi au uitat un lucru: restricţionarea din România nu a avut loc pe baza înregistrării unor cazuri de agranulocitoză în ţara noastră. Unele voci care susţin algocalminul – medicamentul emblemă al industriei farmaceutice româneşti până la scoaterea lui din categoria OTC – cred chiar că întreaga campanie împotriva algocalminului s-ar datora, de fapt, încercării de a detrona un medicament autohton ieftin şi a înscăuna medicamente analgezice străine, mult mai scumpe.
Indiferent de ceea ce spun adversarii sau susţinătorii algocalminului, un lucru este clar: povestea restricţionării medicamentelor pe bază de metamizol este cel puţin ciudată. De ce? Fiindcă riscul apariţiei agranulocitozei nu este acelaşi în toate ţările, fiind determinat şi de caracteristicile populaţiei din anumite zone geografice. Aşadar, ceea ce e bun pentru unii s-ar putea să fie rău pentru alţii. De aceea, dacă într-o ţară sau în mai multe se scoate un medicament din circuitul farma, nu neapărat medicamentul trebuie scos din piaţă de tot. Şi nu este numai cazul metamizolului, ci şi a altor substanţe active, inclusiv al unor vaccinuri. În plus, cred că industria farmaceutică românească are şi ea medicamentele sale care-i fac într-adevăr cinste. O să spuneţi că sunt mult prea pro-medicamente româneşti. Nu e adevărat! Subsemnata a primit chiar numeroase mail-uri care avertizau asupra „medicamentelor care ucid”, pe lista neagră aflându-se atât medicamente româneşti – spre exemplu, Algocalmin cât şi străine – de pildă, Aulin.
Anca Crupariu, ofiţerul de presă al ANMDM, ne-a explicat că: „Metamizolul este un analgezic antipiretic, fiind un derivat de pirazolonă. La mijlocul secolului XX s-a constatat că derivaţii pirazolonici se asociază cu cazuri de agranulocitoză, cele mai multe fiind asociate aminopirinei. Metamizolul, cu o structură chimică asemănătoare aminopirinei, a fost asociat, de asemenea, cu raportări, rare, de agranulocitoză, dar potenţial fatale. Primele raportări au apărut în literatura de specialitate în 1946,1952, 1963. Drept urmare, în SUA, Australia s-a restricţionat utilizarea metamizolului, iar ţările din nordul Europei, Danemarca, Suedia şi Norvegia au interzis chiar acest medicament. În perioada 1980-1986 s-a efectuat un studiu internaţional pentru agranulocitoză şi anemie aplastică (Studiul Boston), pe 107 milioane persoane din Germania, Italia, Spania, Suedia, Ungaria, Israel. S-au semnalat 257 cazuri, ceea ce însemna per global 2,4 cazuri la un milion de subiecţi înrolaţi în studiu. În Germania s-au raportat 1,1 cazuri la 1.000.000, în timp ce în Ungaria, Bulgaria şi Italia nu s-a raportat nici un caz. Nu se cunoaşte explicaţia pentru diferenţele de ordin geografic privind riscul metamizolului.
„Nici un medicament nu este lipsit de reacţii adverse, important este ca raportul beneficiu pentru pacient – risc de reacţii adverse grave să rămână pozitiv.“ – Anca Crupariu, farmacist specialist, ofiţer de presă al ANMDM.
La noi, indicaţiile terapeutice aprobate pentru Rezumatul Caracteristicilor Produsului sunt: durere acută severă, când alte medicamente nu sunt indicate, combaterea febrei, când este refractară la alt tratament. Aceste indicaţii terapeutice sunt în conformitate cu cele aprobate în alte state UE. În România nu s-au semnalat niciodată la Centrul Naţional de Farmacovigilenţă al ANM/ANMDM cazuri de agranulocitoză. Pentru alinierea la măsurile de precauţie luate şi de celelalte state europene, prin Hotărârea Consiliului Ştiinţific al ANM nr. 7 din martie 2010 s-a decis schimbarea modului de eliberare de la OTC la P-RF (prescripţia rămâne în farmacie). Atragem însă atenţia, încă o dată, că în România nu s-au semnalat cazuri de evenimente adverse grave, de tipul agranulocitozei, la metamizol, decizia luată de Consiliul Ştiinţific al agenţiei fiind numai de prevenţie şi respectiv de micşorare a unui consum exagerat al acestui medicament (în 2009 se afla pe primul loc în vânzări, în 2010 a scăzut la locul doi).” Acesta e un caz clar în care, dacă alţii au hotărât că un medicament e periculos, nu înseamnă că trebuie să îi urmăm orbeşte. Ceea ce nu înseamnă nici să nu ţinem cont deloc de experienţa negativă a altor state privind efectele adverse ale unor medicamente. Să nu uităm că, în ultimii ani, pe baza deciziei Committee for Medicinal Products for Human Use – CHMP al EMA, ANMDM a retras din farmacii medicamentele care conţineau următoarele substanţe active: Sibutramină – în ianuarie 2010 – conţinută de Reductil, Minimacin etc., utilizată pentru pierderea greutăţii, dar asociată cu un risc cardio-vascular crescut, risc considerat mai mare decât beneficiul scontat; Rosiglitazona – în septembrie 2010 – conţinută de antidiabetice Avandia, Avandamet, Avaglim, dar asociată cu un risc crescut de infarct miocardic, de accident vascular cerebral, considerat a depăşi beneficiul ca medicament antidiabetic şi Meprobamat – ianuarie 2012 – substanţă activă utilizată de aproximativ 50 de ani ca medicament cu efect sedativ, asociată, în cazul tratamentelor de lungă durată, cu riscul de dependenţă, de supradozare, risc de comă şi deces.
Medicamentele intră în piaţa româneascăpe baza a trei proceduri:
Procedura centralizată, adică autorizare de către Agenţia Europeană a Medicamentului – EMA, recunoscută de oricare dintre statele membre, Procedura naţională şi Proceduri europene. Dosarul de autorizare cuprinde date referitoare la: calitatea medicamentului, demonstrată prin documentaţia chimico-farmaceutică şi biologică trimisă, eficacitatea şi siguranţa în administrare, demonstrate prin studiile clinice pe subiecţi umani, prin monitorizarea adecvată a reacţiilor adverse în timpul studiilor. Apoi documentaţia este evaluată în conformitate cu ghidurile europene în domeniu, permanent actualizate. Sunt două proceduri europene de autorizare: Procedura de Recunoaştere Mutuală (MRP) şi Procedura Descentralizată (DCP). MRP este urmată dacă un medicament a fost deja autorizat într-un stat membru, deţinătorul de APP poate solicita recunoaşterea acestei autorizaţii şi în alte state ale UE declanşând MRP. Procedura descentralizată (DCP) este valabilă în cazul unui medicament care nu a mai fost autorizat până la acel moment în UE, iar aplicantul doreşte obţinerea unei autorizaţii de punere pe piaţă în mai multe state membre în acelaşi timp. Toată activitatea de autorizare prin proceduri europene la acest moment reprezintă aproximativ 2/3 din activitatea de evaluare-autorizare desfăşurată în cadrul ANMDM.
De curând, zece noi cazuri de bebeluşi au fost internaţi la Spitalul de Pneumologie Marius Nasta din Capitală din cauza reacţiilor adverse apărute după ce au făcut vaccinul anti-TBC, un vaccin importat din Danemarca. Medicii spun că problemele apar chiar şi după câteva luni de la vaccinare. Copiii internaţi au între trei și şase luni, unii dintre ei aveau reacţii adverse serioase. La Marius Nasta, din martie până acum, alţi 50 de bebeluși au fost trataţi din cauza unor reacţii adverse induse de vaccin. La nivel naţional au fost raportate 115 cazuri de bebeluși la care au apărut reacţii adverse. Autorităţile au retras între timp vaccinul de pe piaţă pentru a-l supune unei cercetări internaţionale, iar părinţii copiilor afectaţi se gândesc să dea statul în judecată.
nr. 12 / decembrie 2012 Tweet


 32,374 afisari
32,374 afisari







One Disappointing Belief On replica watches Shown
Five Different Simple And Easy Details About replica watches Defined
Va felicit pentru articol.
Respectul meu pentru doamna Anca Crupariu.
Un articol interesant. Eu unul sunt contra medicamentelor.
Zagraj ze mną, odwiedź ten serwis, czekam.
Kto chce zagrac ze mna online? Znam strone bez oplat.
Wypożyczalnia aut osobowych